Curso de Eletrônica – Introdução aos Semicondutores – 01
Introdução aos Semicondutores
Os materiais semicondutores são materiais de extrema importância na ciência da Eletrônica. Com essa série de tutoriais pretendemos abordar suas características, aplicações e destacar sua importância para a construção dos mais variados tipos de componentes e circuitos eletrônicos, tais com diodos, transístores, circuitos integrados, e muitos outros.
Porém, antes de entrarmos em detalhes sobre o funcionamento dos materiais semicondutores, precisamos fazer uma pequena revisão de física atômica básica, pois o entendimento de como funciona um átomo, elétrons, bandas de valência e de condução, e de outros conceitos físicos são de suma importância para nossos estudos.
Átomos
Um átomo, que é a menor parte que constitui um elemento químico, é constituído por diversos tipos de partículas, sendo as mais conhecidas:
- Elétron
- Próton
- Nêutron
O elétron possui carga negativa (-), o próton possui uma carga de igual valor, porém positiva (+) e o nêutron não possui carga.
Os prótons e os nêutrons são encontrados no núcleo do átomo, que é uma região densa e central, enquanto os elétrons são encontrados na eletrosfera, uma região ao redor do núcleo, dispostos em órbitas localizadas em distâncias distintas do núcleo.
Um átomo neutro não possui carga elétrica, pois o número de prótons é igual ao número de elétrons, balanceando a quantidade de cargas.
Elétrons: Camadas
Os elétrons (e–) estão dispostos em camadas (ou níveis de energia), a partir do núcleo, e cada camada possui um número máximo de elétrons que pode abrigar.
As camadas são nomeadas pelas letras K, L, M, N, O, P e Q, ou ainda pelos números quânticos principais 1, 2, 3, 4, 5, 6 e 7. A tabela a seguir mostra o número máximo de elétrons que cada camada comporta:
| Camada | K | L | M | N | O | P | Q |
| nº de e– | 2 | 8 | 18 | 32 | 32 | 18 | 8 |
Cada camada consiste em uma ou mais subcamadas, e cada subcamada consiste em um ou mais orbitais atômicos.
Subcamadas
Cada camada possui uma ou mais subcamadas, as quais são compostas por orbitais atômicos. Na tabela a seguir vemos as subcamadas possíveis:
| Subcamada | Nº máx. Elétrons | Onde está presente |
| s | 2 | Em todas as camadas |
| p | 6 | A partir da segunda camada |
| d | 10 | A partir da terceira camada |
| f | 14 | A partir da quarta camada |
| g | 18 | A partir da quinta camada (teórica) |
Os elétrons em uma mesma subcamada possuem exatamente o mesmo nível de energia.
Elétrons – Camada de Valência
Somente a última camada (mais externa) pode se apresentar incompleta em um átomo, e essa camada é chamada de “Camada de Valência”
Os elétrons na camada de valência são mais energéticos, sendo os responsáveis pelos fenômenos químicos e elétricos dos materiais, podendo participar de ligações químicas, como ligações covalentes.
Átomos com a camada de valência completa são os mais quimicamente não-reativos (gases nobres).
Átomos com apenas um elétron nessa camada, ou com 7 elétrons (faltando apenas um para completar a camada), são os mais reativos.
Um elétron na camada de valência pode absorver ou liberar energia na forma de um Fóton (assim como os elétrons em camadas mais internas).
Somente a última camada (mais externa) pode se apresentar incompleta – não é inteiramente verdade; alguns átomos possuem configurações eletrônicas peculiares.
Níveis de Energia e Bandas Proibidas
Cada camada orbital possui seu próprio nível de energia específico.
Assim, elétrons viajando em uma camada possuirão o nível de energia dessa camada.
Os níveis de energia para cada camada aumentam conforme nos distanciamos do núcleo do átomo.
O nível de energia mais elevado em um átomo é o da camada ou banda de valência (onde encontramos os elétrons de valência).
O espaço entre os orbitais é chamado de Banda Proibida.
Os elétrons podem saltar de uma camada para outra se absorverem energia suficiente para atingir o nível de energia da camada seguinte, adquirindo energia potencial no processo.
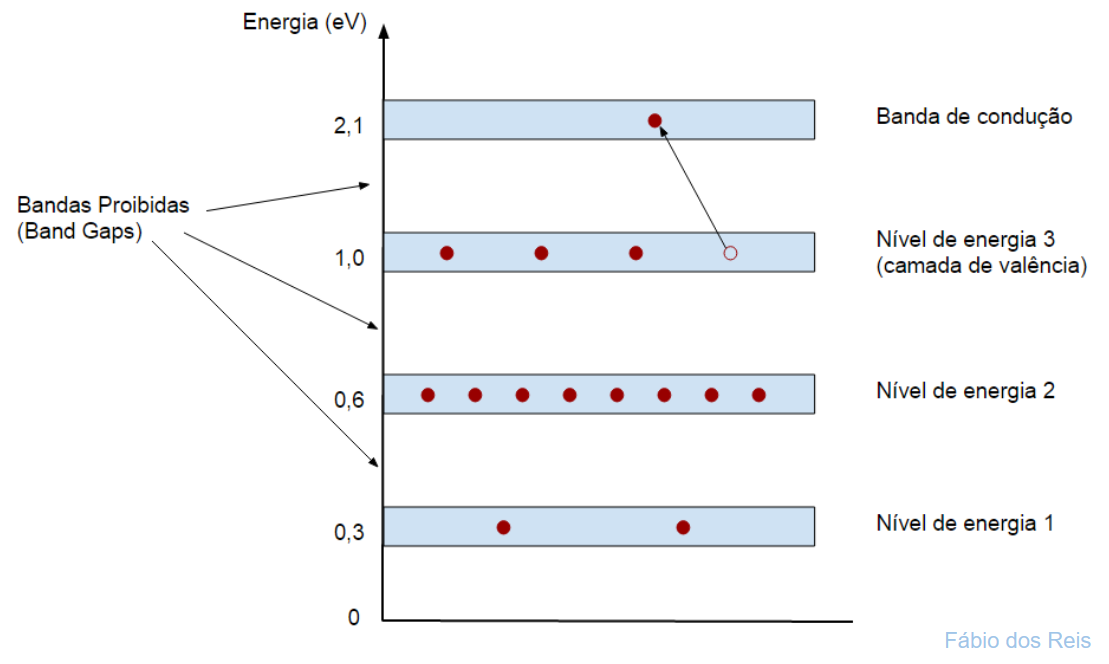
Níveis de Energia e Bandas Proibidas em um átomo de Silício
Níveis de Energia
Por exemplo, na figura anterior, para que um elétron salte do nível de energia 2 para o nível de energia 3 (camada de valência), ele terá de absorver um valor de energia igual à diferença entre os níveis de energia das camadas, ou seja:
| 1,0 eV – 0,6 eV = 0,4 eV |
Isso pode ser conseguido pela aplicação de luz, calor ou ainda de energia elétrica.
Se um elétron de valência absorver energia suficiente, ele pode saltar para a banda de condução.
| Curiosidade: um elétron-volt (eV) é uma unidade de energia que corresponde a aproximadamente 160 zeptojoules (zJ) = 1,6 x 10-19 joules. |
Banda de Condução
Na banda de condução os elétrons podem se mover livremente e viajar dentro de um sólido.
Quando um elétron salta para a banda de condução, ele é liberado do átomo e não segue mais seu caminho orbital. Ele pode se mover livremente dentro do material semicondutor e dizemos que está no “Estado Excitado”.
Eventualmente esse elétron irá liberar a energia absorvida na forma de luz ou calor e retornará ao seu nível de energia original na camada de valência.
Quando um elétron salta da camada de valência para a banda de condução, ele deixa um vazio na ligação covalente chamado de Lacuna, cujo tempo de existência é chamado de Tempo de Vida.
Os elétrons livres se localizam nas órbitas da banda de condução, enquanto as lacunas ficam nas órbitas da banda de valência.
Na parte 02 do tutorial sobre Semicondutores vamos abordar as noções de Condutores, Isolantes e Semicondutores.
Quer aprender tudo sobre Eletrônica? Minha dica é o livro Eletrônica – Para Autodidatas, Estudantes e Técnicos – 2ª Edição, de Gabriel Torres, que você pode adquirir em formato digital com preço promocional clicando na imagem a seguir:






Escreva um comentário