A água conduz corrente elétrica ou é isolante?
A água conduz corrente elétrica ou é isolante?
Essa é uma dúvida muito comum. A maioria das pessoas pensa que a água é um bom condutor de eletricidade, principalmente pelo fato de que no dia-a-dia testemunhamos ocorrências casuais como levar um choque elétrico com os pés molhados, ou ainda casos trágicos com pessoas sendo eletrocutadas durante enchentes em que há danos à rede elétrica. Desta forma, é fácil pensar-se que a água é um bom condutor de corrente elétrica – mas a realidade não é bem assim.
A água destilada (pura) é um isolante muito eficiente, pois possui uma resistividade muito elevada. Porém, há um mecanismo de condução elétrica, muito fraco, baseado no fluxo de íons no líquido – não fluxo de elétrons, mas de íons. Esse fenômeno se dá pelo mecanismo de Autoionização, que permite a formação de quantidades (ínfimas) de íons de forma espontânea na água.
Autoionização da água
A autoionização é uma reação de ionização que ocorre na água pura ou em uma solução aquosa, na qual uma molécula de água, H2O, se torna um íon OH– (ânion hidróxido), por meio da perda de um núcleo de hidrogênio (desprotonação). Esse núcleo então protona (se une) com outra molécula de água, formando um cátion aquoso Hidrônio, H3O+.
A figura a seguir ilustra esse processo:
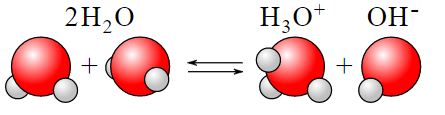
Imagem: Wikimedia Commons
A concentração desses íons na água, determinada experimentalmente, é de 1:10-7 – um par de íons para cada 107 moléculas de água. Assim, em um litro de água temos, aproximadamente, 6 x 1016 pares de íons formados por autoionização. Trata-se de uma razão de 1 para 560 milhões – para cada íon formado, temos 560 milhões de moléculas de água não ionizadas. É uma quantidade realmente pequena, praticamente desprezível, que não permite a passagem de uma corrente elétrica pela água.
Tentando medir corrente na água
Se conectarmos uma bateria, de tensão conhecida, a dois eletrodos de cobre (ou outro metal condutor), posicionados a certa distância dentro de uma cuba com água pura, e tentarmos medir uma corrente nos fios conectados aos eletrodos, usando a Lei de Ohm vamos descobrir que a água apresenta uma resistência elétrica de cerca de 18,2 x 106 Ω/cm (18 MΩ por centímetro) – muito elevada.
Entre os eletrodos, dentro do líquido, íons H3O fluem em direção ao eletrodo negativo, e os íons OH– vão em direção ao eletrodo positivo. Quando os íons entram em contato com os eletrodos, transferem ou recebem um elétron, de modo que o íon se recombina de volta em uma molécula normal de água, H2O.
Porém, essa taxa de recombinação é tão baixa que, para todos os efeitos, a água pura age como um perfeito isolante.
E a água com impurezas?
Tomemos como exemplo a água salgada. Nesse caso, adicionar compostos iônicos na forma de sais, como o sal de cozinha comum (NaCl, Cloreto de Sódio), aumenta a concentração de íons dentro da solução, pois o sal se dissocia em íons Na+ e Cl–.
Cada grama de sal de cozinha adicionada à água introduz cerca de 2 x 1022 íons na solução. Esses íons agirão como portadores de cargas, diminuindo consideravelmente a resistência elétrica da solução para algo abaixo de um ohm por metro (1Ω/m). A resistividade da solução diminui conforme a concentração de íons aumenta.
Neste cenário, a solução irá se comportar como um condutor de corrente elétrica, e seremos capazes, por exemplo, de acender uma lâmpada conectada em série em nosso circuito de exemplo. Lembrando que, como a quantidade de íons positivos e de íons negativos é a mesma, a água, no geral, continuará com caráter neutro, apesar da condutibilidade aumentada
O mesmo se dá na presença de outros tipos de substâncias dissolvidas, porém com concentrações iônicas diferentes de acordo com a substância.
Conclusão
A água pura, destilada, possui uma resistência elétrica tão grande que podemos considerá-la como uma substância isolante, mesmo se levarmos em conta a produção espontânea de íons por autoionização.
Já a água com algum tipo de impureza dissolvida, como por exemplo sais, bases ou ácidos, ou mesmo água comum de torneira, possui uma quantidade de íons dissociados muito maior, tornando-se eventualmente uma substância boa condutora de eletricidade. Seu grau de condutibilidade vai depender do tipo de substâncias presentes em solução, assim como de sua concentração.





Muito bom eu gostei de todas as aulas
Valeu André!
Eu gostei muito do curso muito bem esplanada as aulas estão de parabéns
Valeu André!